现代免疫疗法的到来,在因缺乏治疗选择性而受限的多种肿瘤类型的治疗中引发了变革,从而成为癌症治疗的新里程碑。免疫检查点抑制剂(ICI)因在许多实体瘤中取得的良好疗效而备受瞩目,包括CTLA-4及其抑制剂、PD-1及其抑制剂等。随后溶瘤病毒、自体细胞免疫剂、双特异性抗体、过继性细胞疗法等都显示出令人鼓舞的效果,癌症治疗领域百花齐放。虽然肿瘤免疫疗法(IO)已经与手术、放化疗、靶向治疗并驾齐驱,成为肿瘤治疗的新“武器”。然而,IO仍有挑战亟待克服。
近日,西班牙马德里HM Sanchinarro大学医院Emiliano Calvo博士在《Cancer cell》杂志上发表的一篇综述中,从三个不同的角度详细讨论了免疫疗法的临床挑战以及如何优化。

DOI:https://doi.org/10.1016/j.ccell.2020.07.004
IO开发趋于饱和
不到10年的时间里,IO在17种实体肿瘤中获得FDA批准57个适应症,其中82%是PD-1/PD-L1抗体。临床研究中,正在开发的IO活性药物数量已从2,030增至3,876,在过去两年中增长了91%,而同期引入的独特IO靶点也增加了77%。尽管数量可观,但近两年批准药物的数量有所下滑,主要集中在实体瘤领域。PD-1/PD-L1领域似乎处于稳定状态,但在过去4年中,活跃的临床试验数量增加了20倍,然而这与患者招募率并不匹配,数据显示,同期PD-1/PD-L1联合试验中纳入的患者减少了70%。从总体上分析,可以认为IO药物开发存在一些饱和信号:包括在临床上测试的创新作用机理相对较少,批准停滞情况以及仅针对某些肿瘤适应症和靶标的研究饱和。
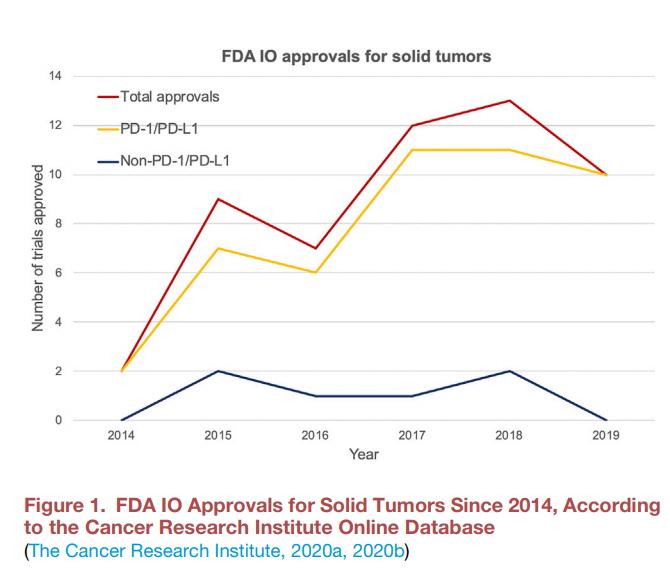
IO临床挑战
抗肿瘤活性
尽管免疫检查点抑制剂的独特在于其实现长期甚至是完全响应的能力,但事实是,大多数患者仍无法从治疗中受益。因此,当务之急是要确定常规放射学评估以外的可靠标志物,以识别IO下患者的肿瘤生物学行为。假性进展者(PP)是可以从ICI中获益的患者,而超进展者(HP)则需要尽早发现,以便立即转为其他治疗。
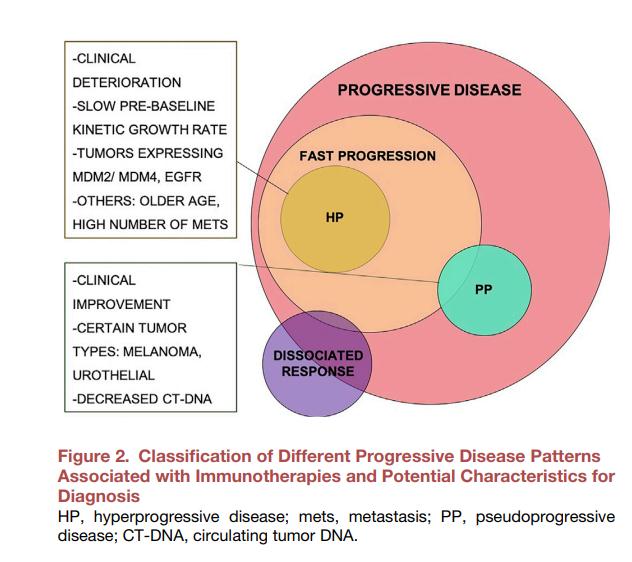
临床试验中的IO终点
已经证明,使用ICI药物获得的生存曲线与常规治疗不同。在与化疗或靶向药物的对比研究中可以观察到,IO在曲线的尾部才能显示出药物获益的最大化。因此,终点选择不当可能会导致试验失败。
临床试验中的功效终点需要捕获这些IO药物更长的活性时机,否则可能会低估该药物的益处。总生存期(OS)虽然是肿瘤学试验中的金标准,但并不能正确地捕捉到IO药物的长期益处。最近引入的新概念——无治疗生存期是理想的癌症治疗终点,因为它考虑了无进展且无需进一步治疗的长期存活患者。其他值得考虑的指标包括生活质量测试或开始下一次治疗的时间。总之,应使用一种更有意义更全面的方式考虑患者福利,而不仅仅是无进展生存期或总生存期。

免疫相关不良事件
与使用常规肿瘤治疗剂相比,IO治疗通常会产生不一样的副作用,包括不同的发作情况、持续时间和严重程度,而免疫毒性经常需要永久性终止治疗。在辅助治疗中,ICI相关的不良事件尤其具有挑战性,因为迟发的、有时甚至是严重的毒性可能导致永久性损害,而这些患者原本可以通过手术治愈。
对IO相关副作用的有效管理取决于症状的早期识别和中和机制解毒剂的迅速启动,例如类固醇或其他免疫抑制剂,而不仅仅是姑息性对症药物。
因此,需要质疑的是,临床试验是否能够通过标准的不良事件通用术语标准(CTCAE)分级来捕获这些特殊的IO功能。此外,有必要建立标准化的客观免疫相关不良事件定义,以获得统一的分类从而避免对药物毒性的误解。威胁生命的ICI引起的过度进展可能也需要纳入CTCAE标准,因为它会对患者造成严重后果。
剂量和时间表
强有力的药效终点结果结合临床反应以及主要的毒性评估,最终决定I期试验的推荐剂量(RD),但大多数ICI剂量查找研究无法鉴定出最大耐受剂量(MTD)或RD。进一步的研究需要解决的是,针对暴露于目标药物的个体患者的剂量调整是否可能比常规剂量获得更好的结果。这将意味着成本节约、为患者带来便利以及通过严格的治疗指数控制潜在地改善药物活性和毒性。
此外,患者继续ICI治疗所需的最佳时间长度仍不清楚。需要开发进一步的随机试验以探索早期ICI中止,再挑战或生物标志物和放射学驱动的ICI开关剂量来回答这个重要的实际问题。
总之,作者对于免疫检查点抑制剂的这些探讨或许能帮助研究人员找到新的突破口,让更多患者从肿瘤免疫疗法中获益。
参考资料:
https://www.cell.com/cancer-cell/fulltext/S1535-6108(20)30365-2







