导语:细胞是人体的基本组成单位,一个成年人体内约有40万亿至60万亿个细胞。干细胞作为具有无限自我更新能力的细胞,能够产生至少一种高度分化的子代细胞。按发育阶段来分,干细胞可分为胚胎干细胞和成体干细胞。根据分化潜能,干细胞可分为全能干细胞、多能干细胞和单能干细胞。鉴于其出色的分化潜能和更新能力,干细胞可用于治疗多种疾病。
成年人的心脏基本不具备损伤修复能力。相比可以修复心脏损伤的两栖动物和鱼类,哺乳动物在修复受损心脏方面有其局限性。许多心脏病会导致心肌细胞和血管细胞死亡,并留下弹性较差的疤痕组织,使心脏功能恶化,进一步导致心脏病患者心力衰竭。
2022年5月12日,来自德国慕尼黑工业大学、瑞典卡罗林斯卡研究所和阿斯利康的科学家在Nature Cell Biology发文,这项研究中,科学家利用干细胞创造了一种使用人类心室祖细胞(Human ventricular progenitors,HVPs)在猪体内再生心脏细胞的新技术。该研究证实HVPs在发育过程中对器官的形成至关重要,可以在需要时变成心脏细胞,从而达到修复瘢痕和受损心脏的积极效果(图1)[1]。

图1 研究成果(图源:[1])
猪心脏在生理上与人类心脏极为相似,因此科学家重点研究HVPs修复猪受损心脏的有效性,从而为后期研究进一步修复人类心脏提供更多线索。主要研究成果如下:
1、为了在单细胞水平上对HVPs介导的心脏修复进行分子解剖,科学家在体外利用成人心脏组织模型来模拟心力衰竭的关键步骤。图2显示HVPs通过CXCL12/CXCR4信号被吸引到心脏损伤部位,在损伤部位进行动态修复。研究结果表明,HVPs通过协调心脏发育的顺序程序能有效促进心脏细胞再生;
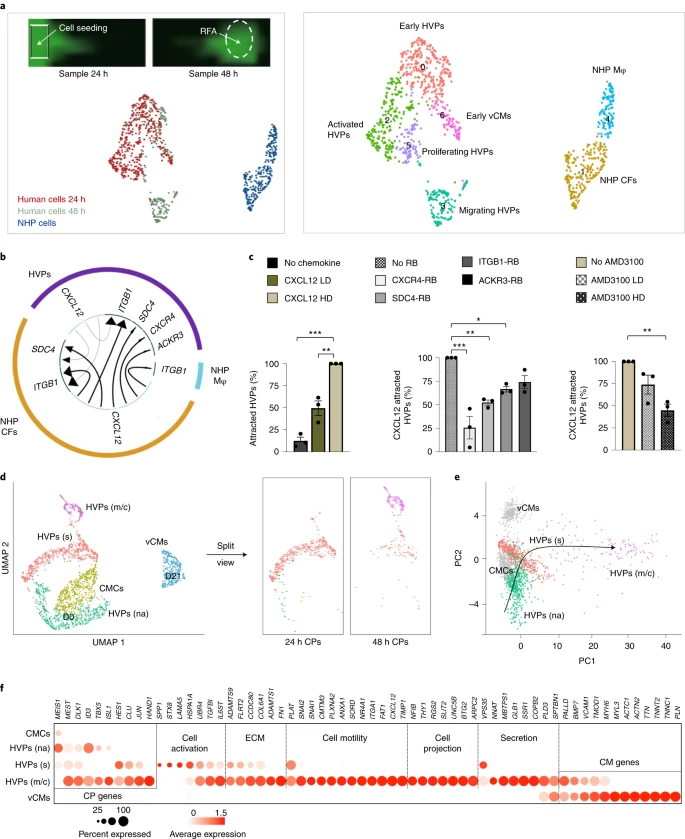
图2 HVP被吸引到心脏损伤部位进行损伤修复的动态过程(图源:[1])
2、为了进一步研究HVP在体内迁移和重新修复受损心肌的能力,研究人员在普遍表达LEA29Y的猪中进行了HVPs移植(LEA29Y是一种人类CTLA4-Ig衍生物,可减弱全身T细胞反应),经CD68免疫检测评估,发现移植后并未出现急性移植排斥反应。此外,以往使用干细胞培养心脏细胞的过程中,患者可能会出现的心律不齐和致命性心律失常等常见副作用,在此项研究中并未出现。
慕尼黑工业大学的Karl Laugwitz教授介绍:“在实验室研究中,我们能够动态展示HVPs如何追踪心脏受损区域,迁移到损伤部位并熟练地为心脏细胞工作,防止形成疤痕组织。”
阿斯利康研究员Regina Fritsche-Danielson博士说:“该技术成功证实心脏新组织的形成。更为重要的是,它改善了心脏功能并减少了疤痕组织,是我们一直在寻找的重建心脏的理想细胞。”
科学家们希望在未来两年内对人体进行临床研究,转化目前的研究成果,为人类心脏病患者开发一种新的治疗方法。若是此项可以修复受损心脏组织的新技术能顺利投入临床使用,那么心脏病患者可能会有更好的预期寿命。
干细胞治疗在修复肺部、卵巢和大脑等器官中的应用
图片 在干细胞研究中,间充质干细胞(Mesenchymal stem cells,MSCs)是当前最为热门的干细胞之一。MSCs具有多向分化的潜能,且免疫原性低、来源广泛,能定向迁移至受损组织部位,重建受损组织与器官,在器官修复领域发挥重要作用。
近年来,科技部每年投入大量资金推动干细胞研究与转化。2022年4月29日,国家科技部发布了2022年度国家重点研究计划《干细胞研究与器官修复》重点专项申报项目指南,涵盖了干细胞治疗新冠肺炎等相关领域(图3)。
图3 通知页面(图源:科技部官网)
随着再生科学技术领域的突破以及与生物技术领域不断的交叉融合,使得目前尚无有效治疗手段的器官损伤或有治愈的可能。下面,让我们结合前沿研究和具体案例,了解干细胞修复器官的诸多应用:
1. 干细胞修复肺部损伤
武汉新冠肺炎爆发期间,部分重症患者会患上肺纤维化后遗症,极大影响患者的生活质量。自疫情爆发以来,干细胞多次被提及并多次应用于临床实验,其疗效及安全性也得到了认可。在武汉,超过200例患者曾接受干细胞治疗。从体外回输的间充质干细胞,可以通过其多向分化的机制,再生出新的肺泡组织,修复受损的肺组织,平衡肺部微环境,在8至10天内实现治愈肺纤维化的目标。
2020年2月15日,科技部生物中心主任张新民在国务院联防联控机制发布会上表示,“从目前看,干细胞治疗能够抑制免疫系统过度激活,通过改善微环境促进内源性修复,可抑制肺部急性炎症进展,缓解呼吸窘迫症状,疗效显著(图4)。”

图4 科技部生物中心主任张新民发布会发言
2. 干细胞修复卵巢早衰
卵巢早衰不仅导致不孕,还会增加心血管疾病、骨质疏松症和性功能障碍的发病风险。目前,大多数治疗方法收效甚微,干细胞移植成为治疗卵巢早衰的研究热点之一。
2021年,发表在Reproductive Sciences和Stem Cell Research & Therapy上的两篇综述均认为,间充质干细胞移植是治疗卵巢早衰中最有效的方法,可显著改善卵巢功能、增加卵泡数量、提高性激素水平、减少颗粒细胞凋亡,可用于治疗卵巢早衰和不孕症(图5)[2][3]。

图5 研究成果(图源:[2]&[3])
卵巢早衰是当今医学的一大难题,目前我国已启动5项干细胞临床研究项目,可深入评价干细胞治疗恢复卵巢功能的安全性和有效性。干细胞治疗卵巢早衰或可成为患者的新选择,为卵巢早衰引起的绝经、不孕不育等疾病带来治愈希望,帮助女性留住年轻芳华。
3. 干细胞修复胰岛β细胞
胰岛β细胞功能异常导致的胰岛素分泌不足,是I型和II型糖尿病的共同特征之一,许多患者也因此需要终生使用胰岛素进行治疗。
2020年3月19日,中科院研究组在Cell发文“Long-term expansion of pancreatic islet organoids from resident Procr+progenitors”,首次坚定了小鼠胰岛中成体干细胞的“身份”,回答了长期以来胰岛中是否存在干细胞的疑问。

图6 研究成果(图源:[4])
该研究成功鉴定了小鼠胰岛中的干细胞类群,将Procr+胰岛β干细胞和血管内皮细胞共同培养,可以再生出具有功能的胰岛类器官。该新器官包含了胰岛的所有细胞类型,在功能、形态、超微结构以及转录组方面,都与真正的小鼠胰岛非常相似,能够迅速地响应糖刺激并分泌胰岛素,为治愈糖尿病提供了一种可能。
4 干细胞修复大脑
科学家曾经认为哺乳动物在进入成年期后,大脑内所有神经元都已经形成,不会新增。直到上世纪60年代才发现,成年人的大脑的某些部位,依然可能产生新的神经元。
2016年6月2日,美国斯坦福大学医学院的Gary Steinberg在Stroke发文证实,干细胞移植技术可显著改善患者中风症状,让患者重新获得行走、运动、讲话等生活技能。

图7 研究成果(图源:[5])
SB623细胞属于MSCs,采集自两名健康捐赠者的骨髓,并通过实验室培养加以修饰增强大脑功能。研究团队选取SB623干细胞作为治疗细胞,将其注入患者因中风而损伤的大脑区域后发现干细胞移植技术可以让患者重新获得基本生活技能。尽管目前的临床结果仅仅在小部分患者身上得到了积极的验证,但是结果却是振奋人心的。该技术逆转了中风症状,有望改变中风患者已被宣判的人生,并可应用于创伤性脑损伤、神经性衰退疾病等多种脑疾病的治疗中。
5 干细胞修复骨关节
骨关节炎是目前骨科领域患病率最高、患者人群最广的一种疾病。作为一种曾经“专属于”老年群体的疾病,近年来骨关节炎却因马拉松等运动成为当代人的常见病。
近年,科研人员成功地分离了人和动物的MSCs,并发现其在体外仍能保持干细胞特性,使其成为了研究的热点。由于MSCs高增殖及多向分化能力,已经被用作潜在的软骨修复再生治疗细胞。
MSCs可以局部再生半月板、软骨内的软骨细胞,从而治疗骨关节炎,或者静脉输注间充质干细胞,刺激患者自身软骨细胞的再生,缓解骨关节炎,恢复骨关节功能。得益于MSCs与各种支架材料有良好的生物相容性,间充质干细胞在软骨修复应用中具有很好的应用前景[5]。
5月8日,中国科学院院士、清华大学教授中国细胞生物学学会理事长陈晔光在《人民日报》撰文,全面地介绍了干细胞的神奇之处和临床应用前景。陈院士表示,未来干细胞最重要的应用或是再生医学,干细胞技术有望用于修复衰老器官,使人延年益寿并享受高质量生活。生命和健康是科学问题,更是每个人都要面对的人生命题。随着研究成果不断出现,干细胞将继续为疑难复杂疾病提供新的治疗策略,为人类健康做出新的贡献。
题图来源:Stem Cell Malaysia,仅用于学术交流。
撰文|露娜
排版|文竞择
参考资料:
[1]Poch CM, Foo KS, De Angelis MT, et al. Migratory and anti-fibrotic programmes define the regenerative potential of human cardiac progenitors. Nat Cell Biol. 2022 May;24(5):659-671. doi: 10.1038/s41556-022-00899-8. Epub 2022 May 12. PMID: 35550611; PMCID: PMC9106586.
[2]Ulin M, Cetin E, Hobeika E, et al. Human Mesenchymal Stem Cell Therapy and Other Novel Treatment Approaches for Premature Ovarian Insufficiency. Reprod Sci. 2021 Jun;28(6):1688-1696. doi: 10.1007/s43032-021-00528-z. Epub 2021 May 6. PMID: 33956339; PMCID: PMC8144118.
[3]Shareghi-Oskoue O, Aghebati-Maleki L, Yousefi M. Transplantation of human umbilical cord mesenchymal stem cells to treat premature ovarian failure. Stem Cell Res Ther. 2021 Aug 11;12(1):454. doi: 10.1186/s13287-021-02529-w. PMID: 34380572; PMCID: PMC8359553.
[4]Wang D, Wang J, Bai L, et al. Long-Term Expansion of Pancreatic Islet Organoids from Resident Procr+ Progenitors. Cell. 2020 Mar 19;180(6):1198-1211.e19. doi: 10.1016/j.cell.2020.02.048. PMID: 32200801.
[5]Steinberg GK, Kondziolka D, Wechsler LR, et al. Clinical Outcomes of Transplanted Modified Bone Marrow-Derived Mesenchymal Stem Cells in Stroke: A Phase 1/2a Study. Stroke. 2016 Jul;47(7):1817-24. doi: 10.1161/STROKEAHA.116.012995. Epub 2016 Jun 2. PMID: 27256670; PMCID: PMC5828512.
[6]刘志刚.间充质干细胞在关节软骨修复中的作用研究进展[J].继续医学教育,2016,30(07):104-106.