帝基生物(DiaCarta),精准分子诊断及液体活检领域领先者,近日宣布其新型QuantiVirus™ SARS-CoV-2 Variants Detection Kit新冠病毒突变株检测试剂盒获得了CE/IVD认证,在全球防疫的关键时刻提供了有效工具 。该多通道定量PCR试剂盒不仅可以检测新冠病毒, 而且还可有效识别并区分所有目前流行中的高危险突变株,包括Alpha(英国)、Beta(南非)、Gamma(巴西)、Delta(印度)、Delta Plus(印度)、Epsilon(加利福尼亚)和Kappa(印度)突变体。
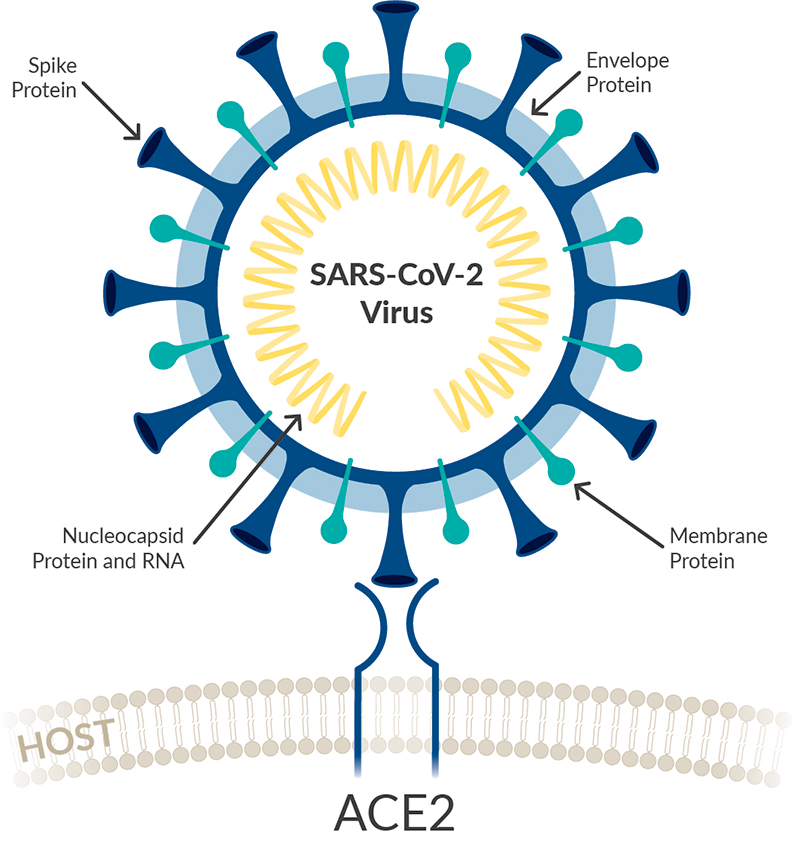
帝基生物(DiaCarta)该创新试剂盒是基于公司多项全球专利XNA分子钳技术的多重qPCR方法,可在常规qPCR仪器上运行。XNA通过与靶DNA序列杂交,作为qPCR反应中的分子钳,高特异性的扩增突变序列,无需二代测序,仅1个小时左右即可检测到目前流行的高危险突变株。

“多种凶悍的新冠突变体来势汹汹,袭击全球。二代测序是检测新冠突变体的主要方法,但是基于NGS的检测方法耗时且昂贵,迫切地需要一种能够快速又经济的平台对突变体进行准确检测。” 帝基生物(DiaCarta)创始人兼首席执行官张爱国博士说,“这款基于XNA技术的创新试剂盒可以实现这两点的完美结合——在精准地检测所有流行中的高危突变毒株同时,提供了更快及更经济的解决方案。感谢欧美CE/IVD论证机构能如此快速地给予我们产品的高度认可, 即时地将该项检测应用于大规模高危险突变株人群识别,为全球抗击疫情作出应有的贡献。”
帝基生物(DiaCarta)同时正在积极的进行美国FDA的紧急使用授权(EUA)认证,全力推进该创新试剂盒高效低成本快速识别高危新冠突变株人群。
关于帝基生物(DiaCarta)
帝基生物(DiaCarta)是一家创新技术的分子诊断公司,通过使用液体活检提供有效的精确诊断来改变病患护理。除已获得FDA EUA批准并名列前茅的两款QuantiVirusTM SARS-CoV-2 Test,新冠核酸检测试剂盒,帝基生物(DiaCarta)还拥有癌症检测系列产品以及提供一系列的检测服务,从单基因QClamp® qPCR 检测到 OptiSeq™ XNA-NGS panel。其新颖的XNA技术具有很高的灵敏度,能将野生型序列嵌合,仅对突变的靶向序列进行扩增。通过使用这项技术,公司已经研发出具有高灵敏度的ColoScape™大肠癌早筛血液检测产品。此外,公司的SuperbDNA™技术,在放大信号时无需进行RNA / DNA提取或扩增,即可提供高灵敏度的检测,为此公司开发了革命性的RadTox™检测产品,该检测产品可个性化定制放射治疗,减少不良反应。DiaCarta(帝基生物)中国总部位于南京市江北新区,拥有第三方临检中心(南京帝扬医学检验所)及ISO3485 大规模GMP生产厂房。同时在美国拥有符合FDA GMP行业标准的生产厂房、及具有CLIA认证的医学实验室。
公司地址:南京市江北新区新锦湖路3-1号中丹生态生命科学产业园B栋2005-2010
联系电话:400-8282-616