我们都知道,病毒无法脱离宿主细胞而存活,如果想要拷贝自己的遗传物质,就需要进入宿主细胞,并借助宿主细胞的DNA或RNA合成、加工工具。不同病毒侵入细胞的方式不同,但大都需要通过结合至细胞表面特定的受体蛋白或脂质结构来实现细胞内化,如果能够阻断这些机制的发生,将有可能开发出预防感染的新方法。
比如甲型流感病毒,是通过病毒表面的血凝素(hemagglutinin,HA)与呼吸道上皮细胞的唾液酸受体结合,吸附于上皮细胞表面,然后再通过内吞作用进入细胞,随后H+经病毒的另一种跨膜蛋白——M2离子通道——进入病毒颗粒内,导致病毒内部pH值改变,HA构象改变并暴露出融合肽,使得病毒与包裹病毒的囊泡发生膜融合,病毒内部的组分因此释放出来,开启后续的转录与复制过程。
新冠病毒则有两种不同的进入细胞的途径。其一是通过衣壳上的棘突蛋白(S蛋白)与人体细胞表面的ACE2(血管紧张素转换酶2)受体结合成复合物,并在网格蛋白的介导下通过内吞作用进入细胞。之后,人体细胞中的蛋白酶将会切割S蛋白,暴露出S蛋白的内层结构S2以及S2’。S2可促使病毒与包裹病毒的囊泡发生膜融合,暴露出病毒的遗传物质并开始复制。另一种途径是当人体细胞表面还有TMPRSS2(跨膜丝氨酸蛋白酶2)存在时,在细胞表面就可对S2’位点进行切割,因此在质膜处,病毒与宿主细胞就可以发生膜融合,并释放出遗传物质。
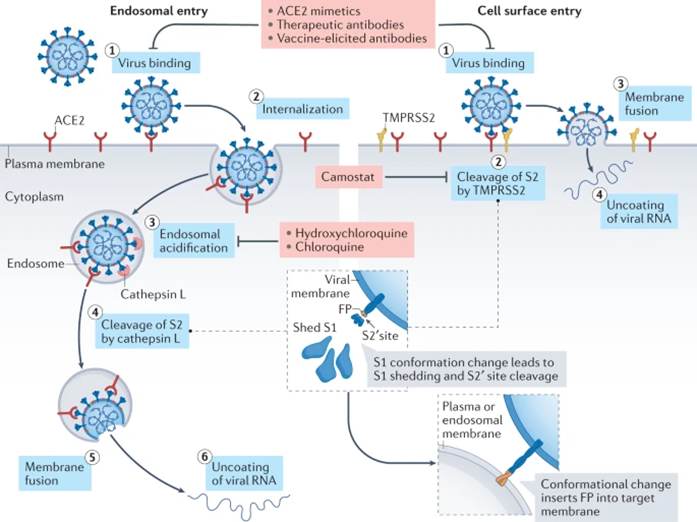
图1 新冠病毒的两种进入途径(图源:[2])
具有高度传染性的埃博拉病毒是一种丝状病毒体,其进入宿主细胞主要是通过宿主细胞非特异性的巨胞饮作用或网格蛋白介导的内吞作用。随后,在宿主细胞表面受体或低pH环境的影响下,病毒表面的三聚糖蛋白(GP)被激活,启动病毒与包裹病毒的囊泡之间的膜融合。
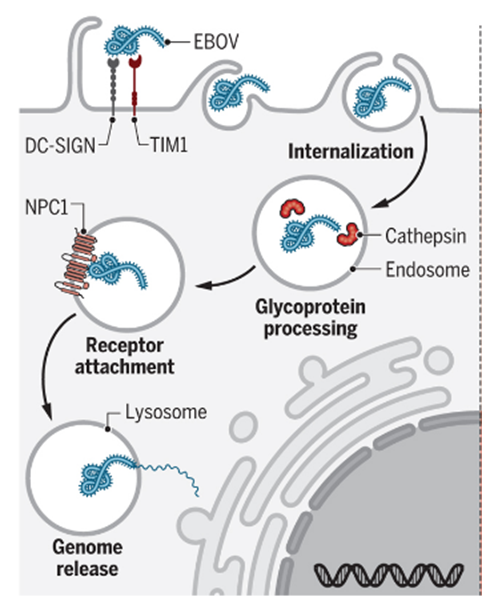
图2 埃博拉病毒进入细胞(图源:[4])
由此可见,膜融合可以算是各种病毒将遗传物质释放到细胞内的“最后临门一脚”。膜融合的过程中,融合孔的形成提供了病毒遗传物质释放的“隧道”。如果能够阻止这一步的发生,就有可能预防病毒的感染。事实上,人体的免疫系统也有朝着这个方向进行努力。当受感染的细胞感知到外来基因组的存在,就会向未感染的细胞发送干扰素分子进行“通知”。干扰素会诱使“接到通知”的细胞产生一种名为IFITM3(interferon induced transmembrane protein 3,干扰素诱导跨膜蛋白3)的蛋白,而这种特殊的蛋白能够有效地阻止甲型流感病毒、新冠病毒和埃博拉病毒等的侵入。然而,这种蛋白的作用机制尚不明了。
为此,海德堡大学的研究人员使用低温电子断层扫描计算机模拟研究了病毒渗透的最后阶段。他们发现,IFITM3能够选择性地对囊泡膜中的脂质进行分选,这改变了囊泡膜的局部脂质组成,进而阻止了融合孔的形成。相关成果以“IFITM3 blocks influenza virus entry by sorting lipids and stabilizing hemifusion”为题发表于Cell Host & Microbe。
图3 研究成果(图源:[5])
研究表明,IFITM3不会影响病毒膜和囊泡膜的融合以及脂质的混合,但是会对胆固醇产生排斥,因此,胆固醇会向无IFITM3的区域富集,原本胆固醇所在的位置则被具有相对正向曲率的脂质取代,这会导致膜中张力的变化,阻碍融合孔的形成。没有了大门,病毒会被一直困在囊泡“牢笼”中,直到被内体-溶酶体系统中的蛋白酶和脂肪酶降解。
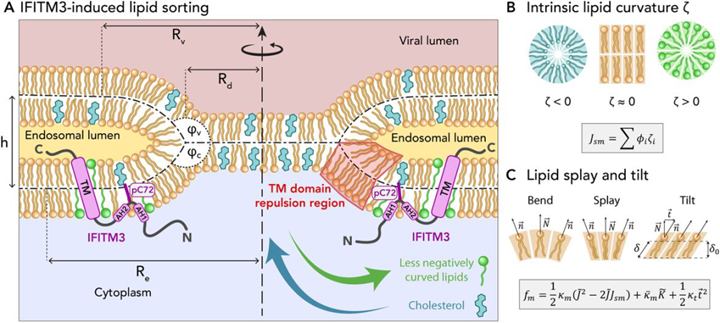
图4 IFITM3引起脂质分选(图源:[5])
研究的资深作者、海德堡大学生物量化中心和海德堡大学医院综合传染病研究中心的病毒学家Petr Chlanda博士表示:“这些病毒被脂质陷阱捕获了,然后被摧毁。”模仿这一机制,研究人员认为或许可以开发出将自身插入病毒膜的脂质分选肽,从而使病毒无法进行膜融合。“这种肽可以是喷鼻剂的形式。”Chlanda说。
在另一项研究中,Chlanda率领团队研究了埃博拉病毒的最后渗透。埃博拉病毒的丝状形态是它的独特之处,这一形态受基质病毒蛋白40(VP40)决定。“我们一直对这种长病毒如何能穿透细胞并通过膜融合释放基因组感到困惑。”Chlanda说。现在,他们得到了答案。研究结果以“The Ebola virus VP40 matrix layer undergoes endosomal disassembly essential for membrane fusion”为题发表于EMBO Journal。

图5 研究成果(图源:[6])
这项研究发现,VP40基质会在膜融合之前发生分解,而该过程是由囊泡内的低pH环境驱动的,这将破坏VP40蛋白和病毒膜之间的静电相互作用,导致VP40基质的分解。如果能阻止VP基质的分解,比如开发病毒基质特异性的弱碱基抑制剂,埃博拉病毒将像甲型流感病毒一样,被困在无法逃脱的陷阱中无法感染细胞。
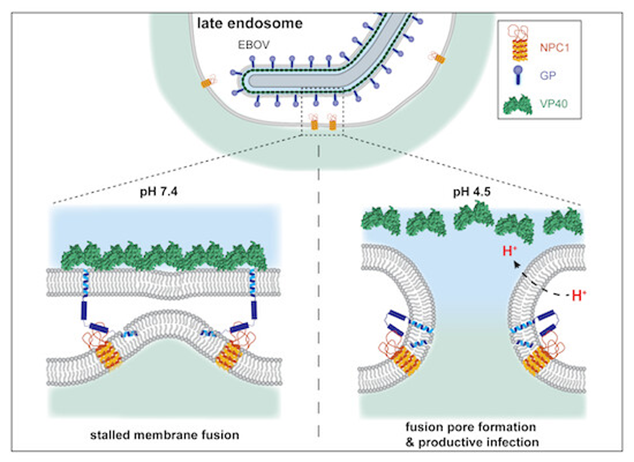
图6 低pH值驱动VP40基质分解(图源:[6])
参考资料:
[1]池晓娟, 王松, 黄一帆, 等. 甲型流感病毒蛋白和遗传物质在宿主细胞质内顺向转运过程及其机制. 生物工程学报, 2012, 28(9):1021−1030.
[2]Jackson, C.B., Farzan, M., Chen, B. et al. Mechanisms of SARS-CoV-2 entry into cells. Nat Rev Mol Cell Biol 23, 3–20 (2022). https://doi.org/10.1038/s41580-021-00418-x
[3]Wang H, Shi Y, Song J, et al. Ebola Viral Glycoprotein Bound to Its Endosomal Receptor Niemann-Pick C1. Cell. 2016 Jan 14;164(1-2):258-268. doi: 10.1016/j.cell.2015.12.044.
[4]Wells AI, Coyne CB. Inhibiting Ebola virus and SARS-CoV-2 entry. Science. 2020 Oct 9;370(6513):167-168. doi: 10.1126/science.abe2977. PMID: 33033203.
[5]Klein S, Golani G, Lolicato F, et al. IFITM3 blocks influenza virus entry by sorting lipids and stabilizing hemifusion. Cell Host Microbe. 2023 Apr 12;31(4):616-633.e20. doi: 10.1016/j.chom.2023.03.005. Epub 2023 Mar 31. PMID: 37003257.
[6]Sophie L Winter, Gonen Golani, Fabio Lolicato, et al. The Ebola virus VP40 matrix layer undergoes endosomal disassembly essential for membrane fusion. The EMBO Journal, 2023; DOI: 10.15252/embj.2023113578






