自2017年首款CAR-T细胞疗法Kymriah被FDA批准用于治疗B细胞急性淋巴细胞白血病以来,截止去年全球共有8款CAR-T产品获批上市。其中,中国国家药品监督管理局批准上市2款,分别为复兴凯特的阿基仑赛注射液(商品名:奕凯达)和药明巨诺的瑞吉奥伦赛注射液(商品名:倍诺达)。而FDA批准的6款产品中,有一款为南京传奇生物研发并成功出海的西达基奥仑赛(商品名:CARVYKTI)。
CAR-T疗法的基本原理并不难理解,即是通过基因转染的方式将从患者或健康供体外周血中收集来的T细胞加以改造,使之表达能够靶向肿瘤细胞的“导航装置”——嵌合抗原受体(Chimeric Antigen Receptor,CAR),等这些升级改造后的“超级战士”在体外扩增到足够的规模,再输回患者体内通过免疫作用消灭肿瘤达到治疗效果。
这套流程说起来简单,但其中的每个步骤都涉及复杂的制造工艺和过程。比如第一步T细胞的收集,如果这一步所得的T细胞纯度不够,比如混入了B细胞,将会导致患者对CAR-T疗法产生抗性。另一个上文没有提到的步骤,是在回输CAR-T细胞之前,需要对患者进行淋巴细胞清除化疗,若清除不够彻底,也将影响疗效。
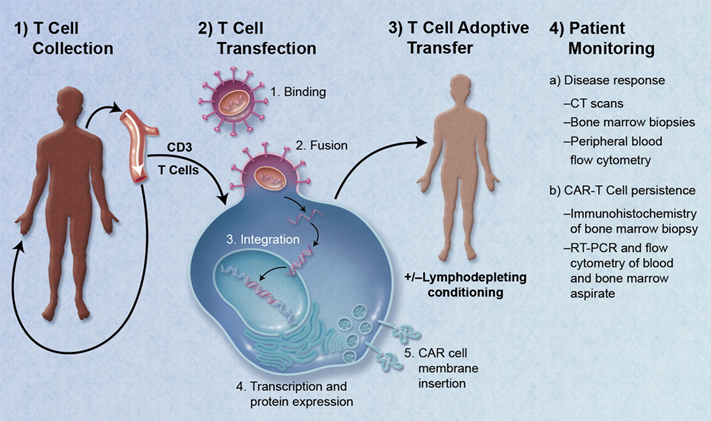
图1 CAR-T疗法流程(图源:维基百科)
CAR-T细胞生产过程中,还有一个关键但较少被谈及的步骤,就是T细胞的激活,它对CAR-T细胞转导效率、扩增速率和分化都有影响。CAR-T细胞转导效率决定了其能否高效识别肿瘤细胞,CAR-T细胞在体内的扩增能力将决定疗效是否持,分化成CD4+ T细胞与CD8+ T细胞的比率也会限制治疗的成功。
这一步骤实际上是通过人工手段模拟了T细胞发育的自然进程。T细胞的激活需要两个独立的信号,其一来自于T细胞受体(TCR-CD3复合物),其二来自于T细胞表面的共刺激分子(如CD28)。自然条件下,这些信号由体内的抗原呈递细胞(Antigen-presenting cells,APC)递送,而CAR-T细胞生产过程中,使用人工APC将更为有效。人工APC甚至可能不是细胞,比如涂有抗体的磁珠。目前,CD3/CD28抗体偶联磁珠,例如Dynabeads,是用于T细胞激活的最常用平台之一。
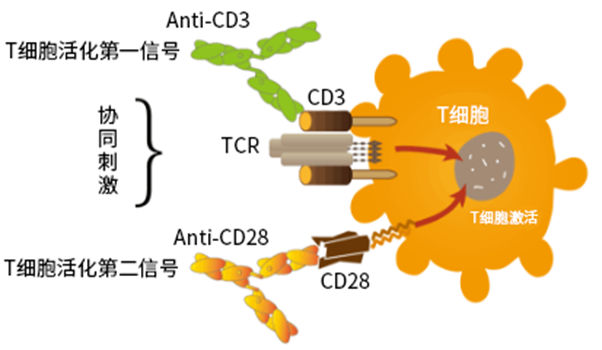
图2 T细胞激活的两大信号(图源:[1])
然而,Dynabeads总是以固定的方式呈现抗CD3和抗CD28,且呈现密度超过生理水平,研究表明这将使T细胞过度刺激和“疲惫”(exhaustion)。Dynabeads按特定的珠子:细胞比例的给药方式,也限制了精确调节T细胞激活第一信号和第二信号刺激剂量的可能性。
另外,癌症患者的T细胞和健康供体的T细胞之间也存在差异,即便面对相同的刺激水平,也会得到不同的结果。如何根据采集所得的T细胞样本的状态,精确调节激活信号的刺激剂量,使得CAR-T细胞产品达到最优功效,也有待进一步的研究。
为此,哈佛大学Wyss生物启发工程研究所David Mooney博士领导的团队在2020年开发了一款可生物降解的APC模拟支架(APC-mimetic scaffolds,APC-ms),以高精度剂量和更接近生理的方式提供刺激。
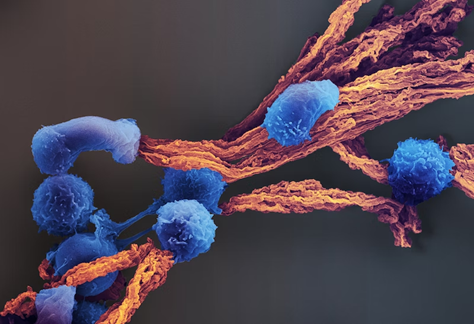
图3 T细胞(蓝色)通过与微支架(橙色)中的纤维相互作用而受到刺激(图源:[2])
在最近发表于Nature Communications的最新研究“Enhancing CAR-T cell functionality in a patient-specific manner”中,研究团队提出了一个根据初始血液样本中T细胞属性来预测最佳刺激剂量的模型。

图4 研究成果(图源:[3])
研究人员从8名健康供体、6名高危急性淋巴细胞白血病(ALL)患者和4名慢性淋巴细胞性淋巴瘤(CLL)患者的血液样本中分离T细胞,并分析了这些T细胞的表型。随后,他们利用APC-ms为T细胞提供不同剂量的抗CD3/抗CD28刺激,并与使用Dynabeads提供刺激的常规方法进行比较。
结果发现,源自患者的T细胞血液样本包含更多的CD8+ T细胞。当使用常规刺激剂量时,癌症患者的T细胞相比健康供体的T细胞更容易出现过度刺激,失去应有功能,且降低增殖能力,且癌症患者的T细胞对刺激剂量的提高更为敏感。
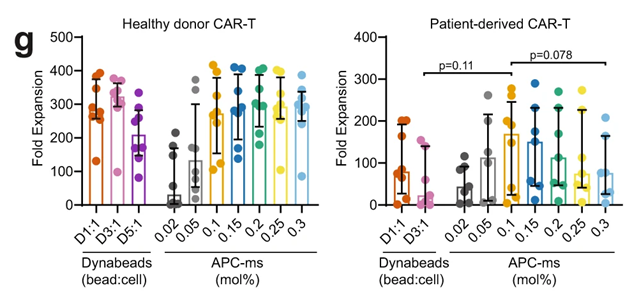
图5 不同方式、剂量提供刺激下CAR-T细胞产品增殖情况(图源:[3])
研究人员还发现,对于患者的T细胞,每个人都存在着一个独特的刺激“最佳剂量”,可以实现功效和增殖的最大化。在一项小鼠体内测试中,不同刺激水平产生的CAR-T细胞产品也表现出了显著不同的抗癌能力。通过APC-ms配合最佳剂量,研究人员使得生成的CAR-T细胞产品产生了更多对肿瘤细胞具有高细胞毒性潜力的细胞以及更多不具毒性的记忆T细胞,CD4+ T细胞与CD8+ T细胞的比率也更加平衡。
研究的作者之一、Dana-Farber癌症研究所肿瘤内科的医学博士Catherine Wu表示:“在CAR-T细胞疗法的开始,我们会对T细胞样本得重要标记物进行指纹识别,因此,可以通过类似的策略为每个患者在APC-ms的基础上实现个性化治疗。”
参考资料:
[1]T细胞活化机理
https://cn.sinobiological.com/research/car-t-therapy/t-cell-activation-mechanism
[2]https://wyss.harvard.edu/technology/biomaterial-scaffolds-for-t-cell-expansion/
[3]Zhang, D.K.Y., Adu-Berchie, K., Iyer, S. et al. Enhancing CAR-T cell functionality in a patient-specific manner. Nat Commun 14, 506 (2023). https://doi.org/10.1038/s41467-023-36126-7
[4]https://wyss.harvard.edu/news/car-t-cell-cancer-immunotherapy-gets-personal/