导语:出生于1986年的X女士,从2岁开始患癌,28年期间先后罹患12种不同类型的肿瘤,其中至少有五种为恶性肿瘤。然而,X女士确诊的肿瘤,在每次治疗后都能快速达到临床治愈水平。针对这种结果,Science发文表示1/80亿的基因突变,使X女士对肿瘤极端易感。同时,这种基因突变改造了X女士的免疫系统,进化出识别并杀死癌细胞的能力。
命途多舛的X女士:全球已知癌症风险最高的人
X女士姓甚名谁,因隐私保护,不便透露,但确有其人。在Science发表的论文中,称其为先证者。先证者指在对某个遗传性状进行家系调查时,其家系中第一个被确诊的那个人。从这个称谓中,我们就能够知道X女士多舛的命途与基因和遗传有关。
01 X女士的诞生:不完美的开端
X女士出生于1986年,时年其母亲26岁,父亲30岁,均健康且非近亲。X女士为足月顺产,但出生时体重、身长低于平均值,新生儿评分为9分(满分10分)。X女士有小头畸形,在出生的头几个月,发育迟缓和轻度精神运动迟缓很明显。但在2017年的体检中,没有发现X女士有精神发育迟滞、肌张力减退、癫痫发作、早衰特征或免疫缺陷的证据。
02 艰难的成长:不是在患癌,就是在患癌的路上
2岁时,X被诊断出左侧耳道胚胎性横纹肌肉瘤Ⅲ期,并接受了放化疗;15岁时,在X股骨、肱骨和尺骨中发现了数个软骨瘤的骨块。同年,诊断出IB期透明细胞宫颈癌伴宫颈外管和宫颈管受累,但无人乳头瘤病毒感染证据,并进行了子宫切除术、双侧附件切除术、近距离放射治疗和外部放射治疗;20岁时,诊断出左侧腮腺的多形性腺瘤,并行手术切除术;21岁时,诊断出低级别梭形细胞肉瘤,接受了左侧乳突切除术和左侧腮腺切除术;21-24岁期间,相继手术去除了几个发育不良痣、一个乳腺脂肪瘤和一个毛母细胞瘤;24岁时,由于多结节性甲状腺肿进行了半甲状腺切除术;26岁时,对一个含有黏膜内腺癌的结肠腺瘤进行息肉切除术;28岁时,切除了一个pT3N0M0直肠腺癌和另一个管状腺瘤;在28岁至36岁,X一直没有出现其他相关病症。
03 病因的深究:无家族史,问题出在哪里?
X女士的高频患癌,且癌症类型层出不穷,不仅让她的父母产生了疑虑,也让她的医生大为震惊。医生觉得有必要对X女士的家族遗传史进行调查,结果发现其母系家族中的女性似乎都很难有孩子:外婆怀孕7次,其中2次自然流产,1次死产且为男孩;1位阿姨连续4次不明原因流产;姐姐在17岁那年,确诊1型糖尿病,婚后经历了3次早期流产。在癌症方面,X女士的叔叔,55岁时确诊结直肠癌;母亲在45岁时确诊左乳浸润性导管癌Ⅲ期,雌孕激素受体阳性,HER2阴性。但是,这些家族史并不能解答X为什么高频患癌。
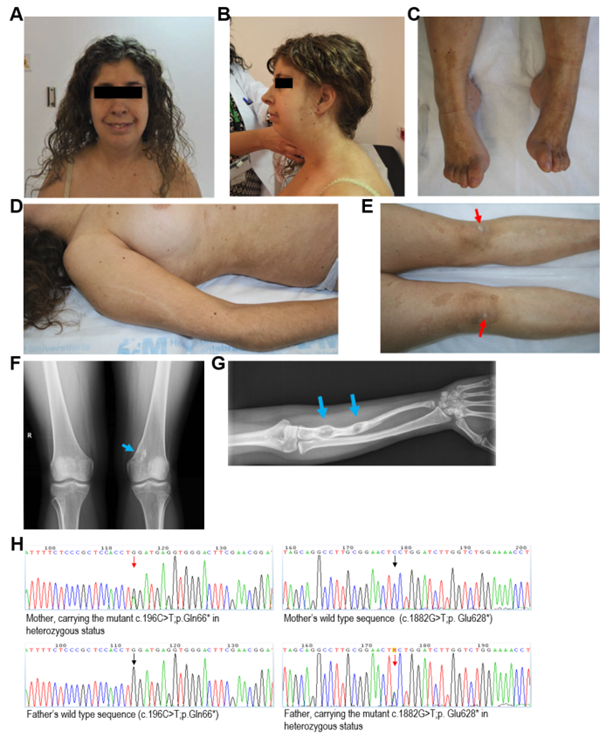
图1 X女士的形态学特征和家庭成员的DNA测序(图源:[1])
在X女士及其家人的许可下,由西班牙国家癌症研究中心领导的一个国际研究小组采集了X女士及其亲属的血液样本,并使用多细胞测序以期找到遗传性肿瘤等相关基因。但是,结果让研究人员大失所望,没有找到遗传性肿瘤的相关基因。考虑到多细胞测序只测了细胞的“平均分”而没有纳入细胞的异质性,研究人员调整策略,使用单细胞DNA测序来观察数千个单个细胞内的基因突变。
最终,研究人员发现了一些奇怪的东西:X女士有一种独一无二的基因(MAD1L1)突变,使她更容易患癌症。X女士的父母虽无血缘关系,却都有MAD1L1等位基因突变,综合导致X女士获得了MAD1L1纯合突变。在MAD1L1基因的两个拷贝中都发生了突变,这在人类中见所未见。X女士是迄今有文献报告的首例MAD1L1纯合突变者。
MAD1L1在细胞有丝分裂、增殖过程中发挥着重要作用。一旦突变会导致细胞染色体数量异常,并造成细胞过度复制。在X身上,MAD1L1纯合突变导致细胞复制功能障碍,并产生了具有不同数量染色体的细胞。研究人员推测X女士患有镶嵌杂色非整倍体(Mosaic variegated aneuploidy,MVA)综合征。
04 反科学经验:X女士的出生堪称奇迹
通常在人类身体的每个细胞的细胞核内都有23对染色体,在每一对染色体中,一个来自人的母亲,另一个来自人的父亲。患有MVA的人在不同的细胞中有不同数量的染色体,就像不同颜色的瓷砖马赛克一样。这种情况可能是由几种不同的基因突变引起的。MVA患者经常会出现发育迟缓、小头畸形(儿童的头部比正常人小)、智力障碍和其他先天性缺陷,也易患癌症。但是X没有智力障碍,并且过着相对正常的生活。
MAD1L1纯合突变会导致胚胎和神经系统发育异常,造成不孕不育、流产、胚胎停育等,动物实验发现对小鼠胚胎是致命的。但X不仅顺利出生,也没有显著智力缺陷,这让研究人员感到不可思议。此项研究的负责人Marcos Malumbre表示:“我们仍然不明白这个人是如何在胚胎阶段发育的,又如何在这些病症下存活的。”
祸福相依的X女士:MAD1L1突变改造免疫系统,识别并杀死癌细胞
X女士的MAD1L1突变造成编码纺锤体装配检查点(Spindle assembly checkpoint,SAC)蛋白MAD1功能异常。在有丝分裂过程中,会经历染色体排列在细胞中线,然后均分至两个新细胞的过程,而MAD1发挥使染色体正确排布的功能,MDA1的失常将导致染色体胡乱分配。X女士大约30%-40%的血细胞有异常数量的染色体,远高于母亲的1.5%和父亲的0.7%。
虽然非整倍性在癌症中的作用尚不清楚,但大约90%的肿瘤带有额外或缺失染色体的癌细胞,高度的非整倍性与癌症的较差结果有关。MAD1L1突变使X女士具有极端的癌症易感性。但是,X女士的免疫系统在对抗癌症时发挥了关键作用,也是其能“反科学”存活的的一大原因。
01 正常细胞“全民皆兵”,应对异常主动出击
X女士的单细胞转录组分析表明正常细胞表现出与炎症反应相关的基因表达增强,包括干扰素和NFκB信号通路,与抗原呈递相关的途径也显著上调。非整倍体诱导细胞自主反应,其特征是抗原呈递增加、翻译和翻译和OXPHOS下调,以及全身性非细胞自主炎症反应。简而言之,X女士体内正常细胞通过上调与炎症反应相关的基因,营造慢性免疫反应环境,可及时识别染色体异常的细胞。
02 武装免疫系统,见一个杀一个
在X女士的免疫系统中,MAD1L1突变导致γδ T细胞表现出活化特性,颗粒酶或杀伤凝集素样受体(如KLRG1)的表达增加。γδ T细胞不仅针对病原体,还针对自身肿瘤和应激细胞,已在体内外多种实体瘤细胞中,显示出强大的肿瘤细胞杀伤力。此外,MAD1L1突变导致B细胞的特异性克隆扩增,增强自然杀伤细胞和T细胞的活化。强大的免疫环境可及时清除异常细胞。
针对X女士免疫系统的变化,此项研究第一作者Carolina Villarroya表示:“A女士的免疫反应似乎因基因突变而变强。MAD1L1纯合突变刺激免疫系统,诱导细胞自主反应。其血浆中特定细胞因子和炎症水平都较高。”Marcos Malumbre表示:“我们有个猜测。MAD1L1纯合突变导致机体不断产生异常细胞。慢慢地,免疫系统能识别染色体数目错误的细胞,形成慢性防御反应。70%的癌症伴有染色体异常。基于这一发现,我们或能利用非整倍性的免疫增强,开启癌症临床治疗新研究。”

图2 Carolina Villarroya(左)和Marcos Malumbres(右)(图源:[2])
参考资料:
[1]Villarroya-Beltri C, Osorio A, Torres-Ruiz R, et al. Biallelic germline mutations in MAD1L1 induce a syndrome of aneuploidy with high tumor susceptibility. Sci Adv. 2022 Nov 4;8(44):eabq5914. doi: 10.1126/sciadv.abq5914. Epub 2022 Nov 2. PMID: 36322655; PMCID: PMC9629740.
[2]https://www.dailymail.co.uk/wires/pa/article-11382861/Case-woman-survived-12-tumours-paves-way-early-cancer-diagnosis.html







