本文转载自“小桔灯网”。
1# 华大基因被合作伙伴“以卵击石”实名举报

2018年6月14日傍晚,王德明以“独孤九剑王德明”的注册名在天涯论坛发出了一篇《举报华大基因伪高科技忽悠欺诈涉嫌贿赂官员,大规模套骗国有资产》的文章,以“国家基因库细胞中心江苏运营中心”之名,向江苏省人民政府举报华大基因。华大基因方面回应称:“纯属无稽之谈、恶意诽谤。”一时引起行业热议。
2# 明德生物上市,POCT市场迎来第三家A股上市企业

2018年7月10日上午,武汉明德生物科技股份有限公司正式在深圳证券交易所中小板上市。作为继万孚生物、基蛋生物之后第三家以POCT为主营业务的A股上市公司。明德生物以1.6亿营收,6000万净利润,排队两年成功IPO,当属年度最幸运的IVD企业。明德生物成立于2008年,是一家专业从事体外诊断试剂及配套仪器(POCT\分子诊断\化学发光\血气等)以及移动心电产品的研发、生产和销售的国家高新技术企业。相信资本市场的力量,将推动明德生物的研发进程和规模经营,进一步巩固和提高其在行业中的优势地位,促进我国POCT产业规模的不断壮大。
3# 4款体外诊断试剂作为上市许可持有人制度试点产品成功落地
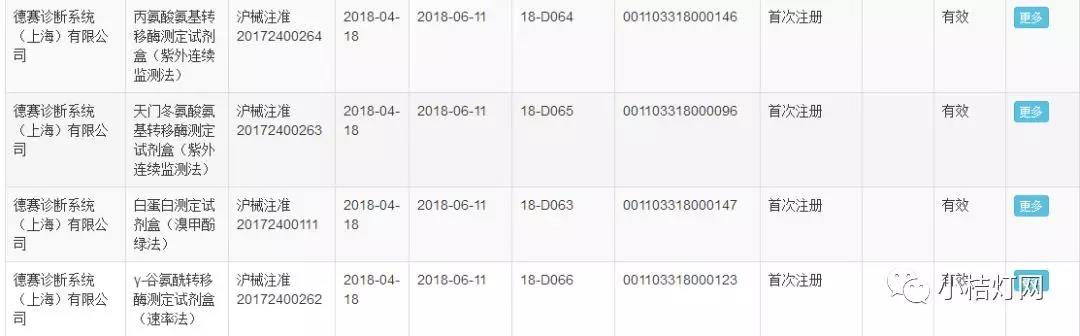
2017年11月,中共中央办公厅、国务院办公厅印发的《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》首次提出要建立医疗器械上市许可持有人制度。该制度在国内外或许并不陌生,但引入我国医疗器械行业却是破天荒第一次。上市许可持有人制度实现了生产许可证与产品注册证的“解绑”,被众多行业人士视为破除医疗器械审评审批体制改革顽疾的重要手段。上海作为首个试点区域,在2018年2月远心医疗公司的单道心电记录仪成为首个落地产品。2018年7月,德赛诊断系统(上海)有限公司委托德赛诊断产品(上海)有限公司生产4款二类体外诊断试剂,从受理到上市,总共用时不到2个月,标志着该制度在体外诊断行业的成功落地!
4# 科美生物完成国内体外诊断领域最大规模私募交易

2018年8月1日,体外诊断化学发光企业北京科美生物技术有限公司宣布完成交易规模近20亿人民币的私募股权重组交易。由君联资本和华兴医疗产业基金共同领投,平安创投、中金康瑞医疗产业基金、上海自贸区基金、弘晖资本、经纬中国共同参与投资。本次交易是近几年中国体外诊断领域规模最大的私募交易。
科美生物成立于2007年,是一家专注于临床医学实验室诊断产品研发,生产,销售和服务的专业化高科技企业。该公司目前主要产品有两大系列,上百个品种。其中临床免疫诊断系统以化学发光免疫技术为平台,可以涵盖各种常见的病毒性传染病,如乙肝,丙肝,艾滋病,梅毒,甲肝和戊肝等;各种肿瘤标志物;甲状腺激素;生殖内分泌激素和糖尿病等。临床生化诊断系统可提供全系列疾病生化诊断产品,包括对各种人体代谢的酶类,各种代谢产物和特种蛋白等项目大类的检测产品。其中,新技术含量较高的特种蛋白类为科美的特色项目。
5# 体检巨头认购ICL行业龙头艾迪康

2018年9月27日,美年健康发布关于下属全资子公司签署境外股份购买协议的公告。宣布批准其下属子公司海美爱投资管理出资2200万美元认购艾迪康控股有限公司5%的股份。美年大健康产业(集团)有限公司是中国最大的体检及健康服务集团。杭州艾迪康是全国跨地区连锁经营的第三方独立医学检验机构,其主要业务模式为在中国境内提供医学检验服务,检测服务包括病理学、遗传学、生物化学、免疫学、分子诊断学、微生物学、微量元素和药物临床试验的检验检测。与金域检验、迪安诊断和达安基因合计约占半数以上的第三方医学检验市场份额。艾迪康的市场份额为17%,综合实力处于行业老三。
6# 迈瑞医疗上市,创业板迎最大IPO

2018年10月16日,深圳迈瑞生物医疗电子股份有限公司在深圳证券交易所成功挂牌上市。此次IPO募资总额为59.34亿元,扣除发行费用后的募资净额为57.52亿元,刷新宁德时代创下55亿的创业板IPO规模记录。迈瑞医疗计划将本次募集资金用于光明生产基地扩建等7个项目。迈瑞医疗主要从事医疗器械的研发、制造、营销及服务,产品覆盖生命信息与支持、体外诊断以及医学影像三大主要领域。迈瑞医疗无论从营业收入还是归母净利润,都是国内毋容置疑的领头羊,公司总部设在中国深圳,在北美、欧洲、亚洲、非洲、拉美等地区的超过30个国家设有39家境外子公司;在国内设有17家子公司,超过40家分支机构,形成了庞大的全球化研发、营销及服务网络。
7# 四款伴随诊断产品密集获批
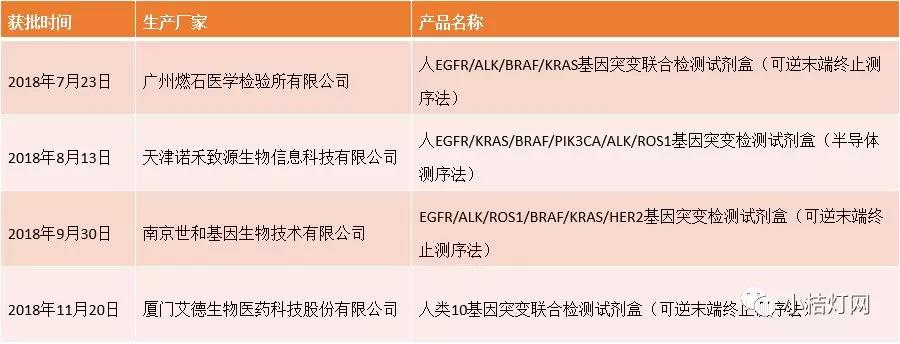
随着对肿瘤分子诊断的深入探索、靶向药物的研究及广泛应用,肿瘤治疗已进入精准医疗的新时代,伴随诊断也迎来重大发展机遇。伴随诊断是一种与靶向药物相关的体外诊断技术,主要通过检测人体内差异蛋白、突变基因等,筛选最佳用药人群,对患者进行个性化医疗,从而改善患者的治疗及预后。目前国内已经获批的伴随诊断产品,绝大多数均基于PCR和免疫组化技术品平台,其特点是只能检测一个或数个确定的药物靶点,目前可以满足临床实践需求,但未来存在一定局限性。2016年以来,美国FDA连续批准多款基于NGS技术的伴随诊断产品。NMPA(原CDFA)同样紧跟国际趋势,2018年以来已有四款产品密集获批,代表NGS伴随诊断产品的突出价值已经获得监管当局的充分认可。
8# 世界首例免疫艾滋病的基因编辑婴儿在中国诞生
2018年11月26日,南方科技大学副教授贺建奎对媒体公布,世界首例免疫艾滋病的基因编辑婴儿在中国诞生。这一轰动消息曝光后仅数小时,就有122位科学家发表联合声明,强烈谴责其未经严格安全伦理性审查即开展胚胎基因编辑;同时,深圳市卫计委表示已启动针对此“基因编辑婴儿”伦理问题的调查。
严格来说该事件不属于体外诊断领域,但受此事件外围影响,华大基因等21家单位,55位 KOL 联名起草发布中国首个《临床单基因遗传病基因检测报告规范》团体标准。该标准规定了临床单基因遗传病基因检测报告应包含的内容以及要求,适用于第三方医学检验机构、医院或大学诊断实验室等出具的临床单基因遗传病基因检测报告。该标准的发布有利于推动临床基因检测报告的规范化,使基因检测报告在不同机构间形成统一标准、提高疾病的诊断效率、减少医患矛盾,进一步促进基因测序行业的健康发展。
9# “4+7”药品集采引发链式反应

2018年12月6日,牵动了无数医药工作者的4+7带量采购招标工作正式结束,作为和药品行业一衣带水的IVD行业,不免人人心生恐惧。诸多行业人士都认为对于IVD行业来说,国家范围的IVD集采肯定会来,而且绝不会太远。其实在IVD行业,像四川、陕西、江苏等地,耗材招投标早已将IVD纳入体系,带量采购方案也不是什么新鲜事。药品降价的空间是压缩了生产、市场、营销、融资四大成本而来的,进而达到既不影响企业获利又让患者受益的目的。那么,IVD 企业的降价,从哪些维度压缩成本值得思考。不仅是集中采购,IVD行业亟待解决的两票制也是我们必须面对的问题。
10# 迈瑞医疗解约200余名应届生

就在2018年最后两天,国产医疗器械行业龙头迈瑞医疗通过电话解约了秋招的200多名签约应届生,并承诺支付5000元赔偿金。华东地区某高校应届生王冠(化名)透露,被解约的学生来自北京航空大学、暨南大学、上海交通大学、武汉大学、四川大学、成都理工大学等60所海内外的高校,多为研发类岗位。12月31日下午,迈瑞通过媒体回应称解约有三方面原因,一是公司进行业务梳理后发现目前需要更多社招而非学生,所以取消了部分原定明年秋季入司的合同,并按合同进行了赔偿;二是社招正常进行,对公司经营没有影响;三是业务现状符合公司预期。
2019年1月2日,A股迎来第一个交易日,迈瑞医疗开盘后一度暴跌近9%,最后收跌至5%。第二天,迈瑞医疗仍然跌幅超2%。第三天略有回升,涨0.26%,报101.58元/股。在1月2日、1月3日两天时间,迈瑞医疗的累计跌幅高达7.23%,蒸发了近100亿元。同时,由于“解约风波”所涉及的岗位大多都是研发岗位,也让迈瑞医疗备受“重销售轻研发”的质疑。
2019年1月9日,迈瑞官方发布声明称经过公司内部进行多次深入研究与谈论,将保持就业协议的有效性,欢迎各位应届毕业生按照原计划到迈瑞就业报道。







