3月21日,Aura Biosciences宣布,欧盟委员会已批准AU-011为首个新型病毒样药结合物(Virus-like Drug Conjugate,VDC)疗法,用于治疗葡萄膜黑色素瘤。该产品此前已被美国FDA授予治疗葡萄膜黑色素瘤的孤儿药称号。
葡萄膜黑色素瘤是一种罕见且在病理学上易误诊的疾病,它也是成年人眼内最常见的原发性恶性肿瘤,其发病率在国外占眼内肿瘤的首位,在国内则仅次于视网膜母细胞瘤,居眼内肿瘤的第二位。早期、体积比较小的黑色素瘤通过联合治疗,包括敷贴放疗、激光和手术,不仅能延长生命,还能保留眼球和视力。但是一旦发生转移(肝脏),中位生存时间约18个月,死亡率极高。
Aura Biosciences是一家临床阶段的生物技术公司,正在开发用于治疗多种肿瘤适应症的新型VDC疗法。Aura计划研发AU-011全眼肿瘤学专利,包括脉络膜转移患者的治疗。此外,利用Aura的技术平台,Aura还在推进将VDC技术应用于其他具有高度未满足需求的癌症,其中实体肿瘤适应症(非肌肉浸润性膀胱癌)患者也在进行1期临床试验(图1)。
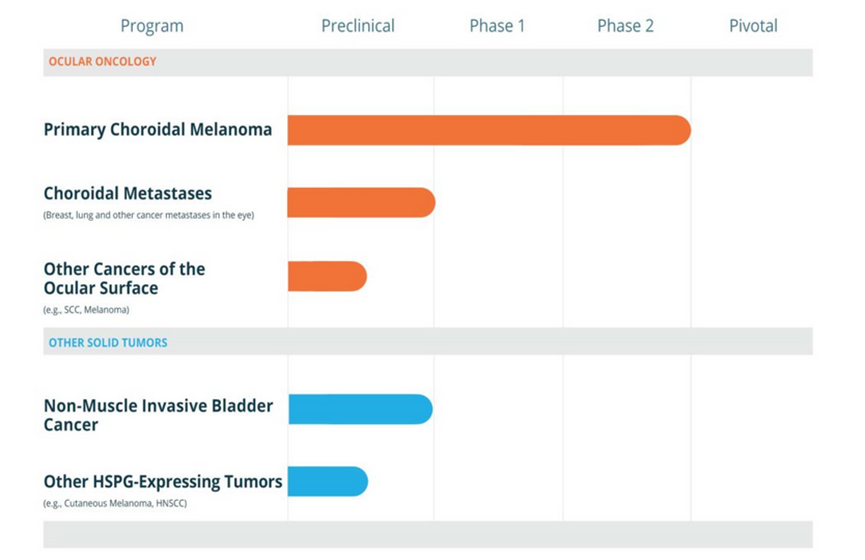
图1 Aura的研发管线(图源:Aura官网)
AU-011药物的创新性。AU-011是一种VDC治疗药物,在临床开发中属于一线治疗,目前正处于2期临床开发阶段。VDC的病毒样成分选择性地结合独特的硫酸肝素蛋白多糖(HSPGs),HSPGs在脉络膜黑色素瘤细胞的肿瘤表面修饰和过度表达,偶联的红外光激活细胞毒性药物用眼科激光激活后,会迅速特异性地破坏肿瘤细胞(图2),导致肿瘤细胞急性坏死并同时激活免疫系统,从而产生长期抗肿瘤免疫效果。

图2 红外光激活后的过程(图片来源:Aura官网)
VDC结合了肿瘤独特特异性,使关键的眼部结构得以保存,有助于保护患者的视力和减少放射治疗带来的长期并发症。AU-011可以借助眼科医生办公室中常见的设备进行给药,不需要进行手术,为患者和医生来提供了一种潜在的微创、更方便的治疗方法。
现在,部分偶联药物已经有相关产品上市,但更多的仍处于临床前和临床早期阶段,其有效性及安全性仍需进一步验证,临床的应用仍存在众多挑战。
撰文|郭亚青
排版|乔维钧
参考资料:
[1]https://aurabiosciences.com/about/overview/
[2]https://aurabiosciences.com/vdc-platform/scientific-presentations/
[3]https://www.biospace.com/article/releases/aura-biosciences-announces-orphan-drug-designation-granted-to-au-011-by-european-commission-for-the-treatment-of-uveal-melanoma-includes-choroidal-melanoma-/





