“客观的讲,我们已经进入中国医药创新的第一方阵”,刘革新说,根据各方评价,无论是产品线布局,在研产品价值,还是研发团队阵容,科伦无疑当属国内第一阵营。5年以后,“我不会这样提,因为我就是第一”。
刘革新的自信,并非妄言空谈,而是实力使然。科伦3年投入13亿,布局347个研发项目,涵盖肿瘤、肝病、糖尿病等10余重大疾病领域,已申报100项,30项为国内首家申报。
2015年,有33个优秀产品获批临床,以数量计,与齐鲁、天晴、恒瑞、豪森并国内五强之列;同年,科伦注射用乳糖酸阿奇霉素/氯化钠注射液获“中国人民解放军后勤部卫生部军队医疗机构制剂批件”,成为国内首家上市粉液双室袋的企业;同时,生物大分子和新型给药系统药物亦首战告捷,西妥昔单抗和紫杉醇白蛋白纳米粒分别获国家食品药品监督管理总局(以下简称“CFDA”)注册受理;而卡巴他赛、巴多昔芬、托法替布、吉非替尼、西格列汀等一系列颇具市场潜力的优秀药物也进入临床,蓄势待发。
物类之起,必有所始。科伦研发成就斐然的背后是其建立的强大研发军团。2012年底,科伦礼聘业界“药研一哥”王晶翼领衔研发。在其主导下,仅仅三年时间,科伦研发团队从125人增长至820余人,至为重要的是,引进的40余位(外籍专家21人)各专业领军人才均是来自辉瑞、默克、礼来、诺华、梯瓦等国际知名企业,从事研发工作多年,实战经验丰富。
精兵强将,奋斗三载,战功赫赫,谁还敢说科伦研发“光说不练嘴把式”?
当年,科伦提出“三发驱动”发展战略时,业界对其“第三发”研发创新不仅关注者鲜,且嗤之以鼻。因为,科伦留给业界的第一印象是,手持成本利器,以凌厉的价格和长袖善舞的资本手段杀伐市场,研发非其所长;其次,江苏恒瑞、正大天晴、齐鲁制药等处于“中国研发第一阵营”的企业,都是研发投入10余年始有所成。所以业界的观点是,科伦入局太晚,即使真的“研发创新”,要开花结果,有年无月。
不过,这一切在将产品和技术创新视为“国之利器”的刘革新眼中,都不足为虑。因为科伦的“高技术内涵药物研发”战略,谓之终极驱动,意在基业长青,怎会无的放矢地出台?其之所以敢于示人,必然如《孙子兵法•始计第一》所言:兵者,国之大事,生死之地,存亡之道,不可不察也。
事实也证明,有关科伦研发的论断确实“不足为虑”,研发创新完全可以“弯道超车”。但问题在于科伦是如何做到的?
精准战略
六七年前,科伦曾启动研发的“战斧计划”:对跨国药企“最有市场生命力、利润最高”的产品进行追踪调研,并按其市场占有率、是否进入医保及抢仿可行性等三大标准,列出了72个重大产品的抢仿计划。但受资金制约,“战斧计划”计划一直未能规模化实施。
2010年科伦上市,在资本助力下,“三发驱动,创新增长”发展战略全面起航,而其引爆点正始于2012年年末王晶翼领军研发。王晶翼应邀加入科伦之初,曾向刘革新提出过这样一个问题:科伦是想做中国医药研发第一方阵,还是中国第一?做到中国第一后,科伦有没有染指世界500强的雄心?刘的回答是:有。
有雄心壮志,有目标,还需有具体的落地战略。刘革新将王晶翼称之为具有企业家思维的科学家,这主要是因为其对医药研发的深刻理解和未来研发趋势的精准判断。
“企业的排名固然重要,但更重要的是,充分了解以美国为代表的国际制药工业历史发展沿革,由此制定符合国情的大型制药企业的研发发展战略,并快速、切实地提升研发水平”,王晶翼说,“从中国医药产业的发展现状来看,中国企业还没有实力如全球制药巨头般,每年投入数十亿甚至上百亿美金去做原创性新药研发,‘梯瓦’先仿制、后创新的发展模式更适合中国大型医药企业。”
众所周知,梯瓦是一家以仿制药研发和生产著称的全球排名前20位制药公司,他向业界证明仿制药可以做大做强。同时,梯瓦也积极投入创新,并且创新药当下已然成为公司主要的利润来源。

科伦研究院院长王晶翼
王晶翼还向E药经理人表示,纵观全球,欧美等发达国家亦深受医疗费用高企的困扰,中国同样面临医保吃紧难题,因此鼓励和支持优秀的仿制药研发是各国政府的首选。从科伦研发所处阶段来讲,科伦需要一个既符合中国国情,又适应企业现实状况的战略。“创新要从仿制起步,没有仿制药做基础,支撑不了创新药物研究,一定要通过仿制药和创新药物的有机结合去支撑企业未来10年的发展。”
深思熟虑之后,科伦的研发战略在2012年的年报中被清晰描绘:通过研发体系的建设和多元化技术创新,对优秀仿制药、创新小分子药物、新型给药系统和生物技术药物等高技术内涵药物进行研发,积累企业基业长青的终极驱动力量。
仿制药作为研发战略的基础,是科伦“弯道超车”的首要发力点。对仿制药的考量是,从国内和国外两个市场出发,针对临床需求尚未有效满足的重大疾病领域进行系统研发。
过去三年,科伦大刀阔斧、精心布局,面向国内市场已立项247个高附加值品种,其中有首仿机会的高达111项,已成功申报100项;面向国际市场,已启动8个项目,3项完成实验室研究,预计2017年申报FDA。
具体而言,品牌仿制药以新型分子靶向抗肿瘤药物、糖尿病药物、抗乙肝病毒等重大疾病领域治疗药物为主;在输液领域,为有效满足临床治疗对输液产品和剂型的需求,在电解质、麻醉、不同疾病状态下的肠外营养支持,以及优化抗肿瘤生物大分子临床使用方法,使其更便捷安全等领域,系统布局了70余项高技术内涵输液和输液剂型品种,其中44项有国内首仿机会;抗生素方面,以克服耐药、去除严重毒副作用及临床用药更安全便捷为首要目标,围绕与川宁技术平台、多室袋技术平台有机衔接的品种、传统优势产品的更新换代品种及新型抗生素等领域立项布局了50余项产品,其中20项有国内首仿机会。
对于这些产品的上市进度,科伦研究院副院长王利春表示,根据国家药审中心及注册司审评审批进度,综合临床研究周期、核心专利时间、药学及临床资源等因素分析,预计未来5年将上市品种80个,20个有首家上市的机会。其中不乏卡文、头孢曲松钠双室袋、注射用帕瑞昔布等诸多重磅品种的首仿上市。
当然,有“染指世界500强”雄心的科伦在系统布局仿制药的同时,更从企业长远发展考虑,积极布局具有创新意义的研发项目。
在王晶翼看来,从仿制到创新,实际上是一个链性思维。现阶段,中国正处在仿制创新(me-too)阶段,近几年上市和申报的产品基本上都是改变结构的me-too类药物,从现在的申报情况看,国内me-too类创新药将会出现“扎堆”上市的态势,所以企业还需要布局代表未来发展趋势的颠覆性、突破性靶点的创新药物;同时,当下生物技术药物继续领跑全球医药市场,全球销售TOP10中7个为生物药,销售市场达1800亿美元,所以科伦也要有所作为。
因此,对科伦而言,首仿、早仿是在满足中国临床需求的同时,争取市场领先地位;小分子创新药物是企业未来的核心竞争力,仿制创新(me-too)可以突破原研专利壁垒实现产品提早上市,改良创新(me-better)和颠覆创新(first-in-class)则有机会参与全球竞争;而生物技术药物则是近年来全球研发的热点领域,虽然科伦介入时间稍晚,但可以直接应用更新一代技术,取得突破性进展;新型给药系统(NDDS)虽多属仿制范畴,但脂质体、微球、纳米粒等高技术内涵产品跟仿困难,一旦拥有就具备了坐享高端市场资本。
创新小分子方面,王晶翼认为,欧美强大的支付体系下,仿制创新药(me-too)难以得到市场认可,但却符合中国国情和广大患者的迫切需求,所以科伦的策略是:面向国内市场以重大疾病、重大药物的成熟靶点为研发目标进行仿制创新和改良创新(me-better/best-in-class),同时加大颠覆性、突破性靶点的布局和研究力度,积极参与国际竞争。目前科伦已经在肿瘤、抗病毒、抗菌、麻醉镇痛等领域启动20项验证靶点的me-too/me-better创新,4项已获得临床候选化合物(PCC)提名,预计2016年申报3项,并完成3~5个新项目PCC提名;同时,面向全球市场已立项启动非验证性靶点项目12个,都是具有国际化潜力的大产品。
生物技术药物方面,科伦在成熟靶点、免疫颠覆性靶点、ADC药物等领域,针对恶性肿瘤、自主免疫性疾病、心血管疾病等重大和多发性疾病领域已布局17个产品,首个生物药(抗EGFR单抗注射液)已成功申报临床。
新型给药系统领域,科伦构建了白蛋白纳米粒、脂质体、长效缓释微球、长效微晶等新型释药系统技术平台,围绕抗肿瘤、糖尿病和精神疾病已启动19个重大仿制和创新项目。其中细胞毒抗肿瘤项目紫杉醇白蛋白纳米粒已成功申报临床。
由此可见,科伦研发以“三发驱动,创新增长”战略为指引,采取以仿制为基础,以创新驱动未来的研发思路,围绕全球重大研制方向、重大疾病进展和重大技术平台,密切跟进国际制药研发进程,推进化学小分子、生物大分子以及新型给药系统的仿制和创新产品线的战略布局已经初见成效,“弯道超车”日趋显现。
不过,“弯道超车”考验的不仅是速度,更是赛车手对赛车的掌控能力。众所周知,对于研发而言,立多少项目,投入多少钱,并不能完全代表企业的研发实力,衡量标准只会是最终能取得多少生产批文。那么,如何保证企业研发项目取得成功?研发风险如何控制?
系统控制
中国医药企业的研发创新本身落后于发达国家,而科伦创新转型又比国内优秀企业晚了近10年,这就要求科伦必须以更快的速度进入研发战场。而速度与“弯道”之间存在天然的“矛盾”,如何平衡研发风险至关重要。
科伦之所以学习“梯瓦模式”,就是从风险控制和长期投入的可持续性角度考量的。虽然“仿制”在探索过程中也需要付出较高的成本,但这种成本付出及风险相对原创要可控得多,关键是回报周期更短。通过仿制快速满足临床需求,抢占市场,进而支撑创新的长周期和高额投入,两者相辅相成。
梯瓦之所以能够以仿制药与创新药巨头比肩,其主要的成功因素就是能够抢仿,而“抢”的基础是准确的立项,从源头开始“抢”。
科伦的研发体系主要划分为“选题立项与合作、药学研究、临床前评价与临床研究、项目注册和综合管理”四大功能体系。其中,选题立项与合作部门是研发的“七寸”,精准的选题立项和对项目的动态评估是科伦控制研发风险的第一步。
科伦“选题立项与合作”功能板块,主要由信息、医学、项目拓展三大部门构成。
“立项无论在哪里,必定来自于临床疾病的治疗需求。”临床出身的王晶翼说,立项首先需要判断的是,某一疾病对人类健康的威胁以及当前是否有有效的临床治疗手段,其次才考虑研发产品上市快慢、企业生产能力、知识产权等要素,而且仿制药与创新药的立项要素并不相同。
此前,科伦的选题立项比较零散,不成体系。王晶翼领衔研发以后,快速重构了完整的研发立项架构和流程。科伦的立项是“全民立项”,医学部负责跟踪全球医学进展并提供创新项目,信息部主要以全球研发数据库为基础系统筛选仿制项目,各专业部门负责人亦会根据自身经验、知识和文献检索提出创新和仿制立项;在立项过程中医学部和信息部会充分评估所有项目立项成立与否的各项要素,并完成初步立项报告。初评通过之后,立项信息会反馈至王晶翼处,由其对项目做最后评价,有些项目可以直接决策,有些项目则还需与市场部、临床医学部联合做进一步评估。
在医学部和信息部进行系统调研和选题立项的基础上,科伦又组建了国际和国内商务拓展部,核心功能是与国内外制药公司、CRO公司、高等院校、科学家直接接触,发现新项目。一旦符合科伦战略,就会纳入科伦标准化的立项程序,进行立项决策。
科伦的仿制药项目很多是在原研药处于三期临床,甚至更早阶段时就展开选题立项,为降低后期研发风险,科伦在紧盯原研药研发进展、审批进度及中国市场变化的同时,还建立了研发项目的动态评估流程,根据原研药的新动态、国家法规变化等对已立项项目进行实时评估,以确定下一步研发策略。
成功立项只是项目研发的正式启动,其后是对研发项目的体系化全程精细管理,这是科伦控制研发风险的第二步,也是保障研发进度的重要手段。
科伦组建了专职的以项目推进和综合管理为主的项目管理部,由研究院分管副院长负责,直接向王晶翼汇报。当项目立项完成后,便会纳入项目管理部的全程管理,包括项目的整体策划、集成管理、分级管理、关键节点管理等等,同时进入由分析中心、合成所、制剂中心、生物技术部、输液药物所、创新中心等多部门组成的仿制和创新药物的药学研究板块及与之交叉衔接的临床前研究与临床评价板块,根据项目特性,确定具体研发方案,并快速推进。
项目的管理和推动是科伦研究院的核心工作。王晶翼说,“我会收到每个部门的项目进展报告,我要求他们定期抄报给我。”首先直报分管副院长,分管副院长会直接解决项目进展中的问题,而王晶翼则是监察一些重大项目的进展,由此形成一个分工又合作的机制。
“关注项目进度是我最核心的工作之一”,王晶翼说,他每天都要根据项目进展情况的反馈,察看各环节之间的相互沟通和推进是否流畅。为此,科伦还设立了三位分管副院长紧盯各研发环节。
为确保项目规范运行,科伦建立了专职的QA部门和法规部,前者检查各部门的项目研发工作是否合规,是否存在风险;后者主要研究国内外专业法规,以便及时调整研发方案和策略。值得一提的是,为突破国外专利垄断并为公司创新成果及未来市场化保驾护航,科伦还从国家知识产权局引进了高端人才组建了高水平的知识产权部,这与梯瓦颇为相似,让知识产权既是“盾”又是“矛”,防守的同时伺机寻找进攻机会。
近年来,创新药已成为国内主流医药企业的研发方向,如何控制创新风险是国内外企业共同面临的重大课题。创新是一项系统工程,创新的高风险必须通过关键技术平台和有效衔接的功能体系建设,用体系的力量在研发的每个环节加以有效控制。
“如果仔细去梳理,就以中国本土医药前十大制药公司来看,其创新团队和技术平台构成与国际主流医药企业的创新体系还是有明显差距的”,王晶翼表示,中国真正的创新药物研究刚刚起步,大多数企业的创新研发,零散而不系统,有些企业的研发机构虽植根美国,但得不到有效管理。
为此,科伦强力实施人才的精兵战略,持续从全球引进相关领域高端领军人才,着力构建与国际水平接轨的创新研发体系,尤其是在创新靶点的选择、成药性评价、临床前研究与临床的有机衔接等关键技术平台,力求达到国际先进水平,以有效控制创新风险。
科伦之所以能够用3年时间完成很多企业十多年才能完成的工作,主要得益于科伦构建了多个与国际接轨的关键技术平台和一套高效运行的研发管理体系。对科伦而言,在研发战略选择上是“梯瓦模式”,本身已整体控制了研发风险;其次,关键技术平台的建成和研发的流程化、体系化以及对关键节点的全面管理和控制确保了研发的顺利进行,也就是说,科伦研发的风险在战略和战术层面都在有效掌控之中。
研发加速器
短短三年,科伦研发可谓脱胎换骨,跃入中国医药研发第一阵营。研发速度之迅猛,研发实力之强悍,令业界震憾。不禁会让人好奇神速之道?
非常之事必待非常之人。“齐鲁制药和科伦的研发,都是我主导之下建设的,我个人研发理念并没有太大变化”,王晶翼说,只是因为企业不同,起点不同,采取的行动不一样而已。科伦属于战略转型,又在高端药物上缺乏经验,如果按常规先建团队、建实验室,再去启动项目做研发,势必错过战略转型的机遇期。
王晶翼来科伦的第一天就已成竹在胸,他用了16张幻灯片向科伦报告未来的研发如何做。三年过去,科伦的研发始终是围绕16张幻灯片的具体实施。
清楚打哪一仗,做哪个品种,做哪个靶点的时候,一切就会变的顺畅。在王晶翼正式就任科伦研究院院长之前,其主导的科伦研发项目就已经提前开始布局了。
“很多事情可以序贯地做,但时间就过去了,很多事情平行地做,工作复杂,工作量大,但可以节省大量的时间”,王晶翼说,科伦的创新和转型本来比众多大型药企落后多年,早在2005年国内的优秀企业就开始启动创新研发,研发管线中已经有一批创新药物,前锋已经进入临床,有些开始获批上市。科伦不能再等时间,让机会溜走。所以为了加快研发速度,一边“让CRO公司为我们做”,另一边快速组建团队,王晶翼第一时间组建的就是负责引进项目的BD团队。
“我会告诉团队,要向什么方向发展,重点关注的靶点是什么,甚至告诉团队在哪里能找到优秀的项目”,王晶翼表示,由此一来,一手抓项目,用CRO公司,一手组建自己的团队,使得整个研发效率大大提升。
“自2002年负责国内药物研发工作以来,中国制药工业的国家政策一直在变革和进步,其方向始终如一,就是仿制与创新药物研究的内涵不断地与国际先进接轨”,王晶翼说。因此,在前期项目顺利起步后,其工作重心便转移到为科伦构建一个与国际接轨的网状研发体系上。
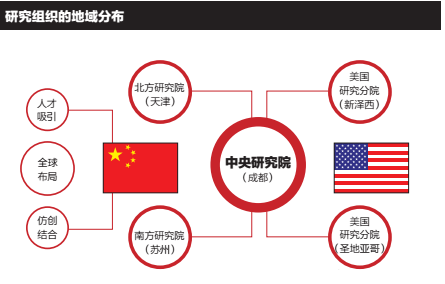
为了快速吸引人才并全方位调用国内外研发资源,2014年科伦在技术和人才资源高度集中的天津和苏州,分别组建了北方研究分院和南方研究分院,成功构建了以成都研究院为核心,苏州、天津研究分院为两翼的国内研发体系。其后,为充分利用国外人才技术资源,使研发体系与国际迅速接轨,2015年科伦又在美国新泽西和圣地亚哥组建了国际仿制药、创新大分子和创新小分子研究分院。
科伦设立研究院分支机构的战略意图是引进人才和技术。“创新是人类最高级的智力活动,没有人才便没有一切。”刘革新说,环渤海湾和长三角地区是中国医药研发人才的两大聚集地,最初科伦是考虑在北京和上海设立研发中心,但因生活成本太高,对研发人员来讲,不如仅离这两个地方半小时车程的天津与苏州来得“实惠”。
通过五位一体的集约化研发机构布局,及各分院间的有机分工和协同配合,大大提高了科伦的研发水平和研发效率,并与国际初步接轨。成都总院作为中枢,承担科伦研发的核心任务,包括创新小分子、生物大分子、国内仿制药、新型给药系统的研发及国际仿制药产业化;天津分院和苏州分院则为国内研发的两翼,主要承担国内仿制药的药学研究任务,未来将逐步建设有特色的单元技术平台;而美国分院的主要功能是承担国际仿制药的研发、生物大分子创新药物的发现、创新小分子药物的分子设计以及海外BD等功能。
经过三年团队建设急行军,科伦研发团队人数增长近7倍,令业界瞠目。但王晶翼依然觉得人手不够,最让他头疼的还是无法快速招到合适的人才。按其规划,科伦国内三大研究院,将在未来三年内形成3×500人的研发团队,可以同时推进3×150个项目。
在研发人才的遴选标准上,王晶翼表示要“又红又专”,他解释说,“红”是综合素养,即为德行层面,如诚实友善、团队意识、吃苦精神、善于学习等内在品质;“专”是专业技能。如果这两条对比,王晶翼说自己更看中第一条。
当然,科伦既然选定了创新之路,在研发人员的待遇上自然不会吝啬,除了颇具竞争力的薪酬、福利之外,科伦又专为研发人员设计了创新型的股权激励计划。
刘革新的爱才之心业界有目共睹,对研发的支持更可谓倾尽全力,充分授权。他曾在内部会议上说:“在研发上,小事听王院长的,大事更要听,叫言听计从,因为我和王院长的心是相通的,我们在伊犁河畔击掌为盟的时候,就对科伦研发全盘战略的路径、方法和策略达成高度共识。”
王晶翼说,科伦对研究院的支持是“要啥给啥”。刘革新去研究院,就是找王晶翼喝酒,从来不问工作,问的最多的就是“晶翼有困难么,还需要什么支持?”王晶翼加盟科伦之初,刘只向王说了一句:“研发就交给你了。”
回想三年来的工作,王晶翼感慨地谈到,“战略制定易,而药物研究体系的全环节、全要素的切实推进不易。虽然管理学上有二八理论,但药物研究的任何一个关键环节出现失误,都可能导致多年的药物研究整体受损。”
为此,在制度上,科伦研究院制定了一整套能够保证研发项目顺利开展的完善制度,确保了研发效率;在体系建设上,科伦快速建成了针对国内外市场、仿制与创新、大分子与小分子及释药系统五大功能体系,并全面与国际制药工业研究水平接轨;在研发机构设立上,形成了以成都研究院为核心,苏州、天津、美国为分支的五位一体,集约化的研发机构体系;在团队建设方面,经过两三年的磨合历练,三军同心,实力强悍。如此“纵横交错”,又相互协同,科伦研发岂能不快?
收获期渐近
4月7日,科伦发布公告称,科伦及其子(分)公司拟投资建设生物医药产业园项目,主要包括“生物技术药物产业基地”和“cGMP国际车间”,预计项目占地面积200亩,计划总投资额为51.61亿元。该项目计划今年开工建设,生物技术药物产业基地预计建设周期为8年,cCMP国际车间预计建设周期为5年。
生物医药产业园项目是继科伦上市六年完成百亿产业投资计划之后的又一巨额投入,业界直叹,科伦“野心”不小。
“三发驱动”战略启动至今,前“两发”已动力十足,风驰电掣。而第三发—研发创新,历经3年低调潜行,已颇具强者风范,如今大手笔投资产业,无疑彰显了科伦对研发的自信与步入收获期的笃定。
生物技术药物产业基地旨在建成以单克隆抗体等生物大分子药物为主的,集药物发现、研发、技术转化和大生产为一体的全产业链平台,涵盖肿瘤、自身免疫疾病、高血脂及眼科用药等重大疾病领域的生物技术药物产品集群。据科伦研究院副院长陈得光介绍,该基地分为中试车间、大生产车间两大工程,其中大生产拟建设6个不同类别药物的生产车间。

自2013年启动生物技术药物研发以来,科伦已立项生物技术药物17项,其中创新项目12项。其中,2015年7月,科伦完成首个项目“重组抗表皮生长因子受体人鼠嵌合单克隆抗体注射液”的IND申报,目前已完成审评。
陈得光表示,根据公司生物技术药物的研发进度,2016年会有3项IND申报,计划以后每年保持2~3项产品的IND申报。而产品的上市时间,预计从2021~2022年开始,每年有1~2个产品上市销售。
而“cGMP国际车间”则是科伦美国仿制药研发计划和创新小分子国际化项目的重要产业化基地,与美国的研发及市场运营直接衔接,该车间将先后建成多条制剂生产线,产品线逐渐覆盖普通和抗肿瘤注射剂、滴眼剂、口服制剂等领域。
2014年10月,科伦启动美国仿制药研发计划,仅用了三个月时间就完成实验室建设,并引进熟知美国仿制药研发的科学家近20人,面向美国仿制药市场已立项并启动研发项目8项,包括普通和抗肿瘤小水针剂冻干粉针,3项已完成实验室研究,预计2017年申报美国FDA,2019年在美国上市。
对于美国仿制药研发,王晶翼表示,每年至少立项5个,有3~5个产品获批,用4~5年时间,形成20个以上的产品群。按照刘革新与王晶翼的约定,未来科伦是要“染指世界500”强的,所以按照王晶翼的说法,“我们研发了那么多好产品,不卖到国际市场那就太可惜了”。
对于生物医药产业园项目,公司董秘冯昊表示,如果完成投资正式运营,预计将实现销售收入145.76亿元,其中生物技术药物产业基地将实现销售收入119.83亿元,cGMP国际车间将实现销售收入25.93亿元。
当然,除了生物技术药物和美国仿制药两大板块前景可期之外,还有一大批产品蓄势待发。未来5年将会有80个产品上市,20个有国内首家上市机会;其中2016年11个,2017年39个,2018年19个,这些产品必将大放异彩。科伦药业总经理刘思川,对产品上市后市场表现情况颇为自信,他说,以科伦的销售实力,在中国必然会取得比原研更好的成绩。
科伦用了3年时间创造了一个研发传奇,让哪些质疑“科伦入局太晚,要待开花结果,有年无月”的流言不攻自破。“只要我插手的,无论你是多大牌,我五年就要超越你”,强悍的刘革新向来崇尚竞争,在输液领域,70万元起家,用了不到10年时间,超越了那些有百年历史的竞争对手;在抗生素领域,资本助力下,成为第一毫无悬念;“新药是一样的道理,让历史告诉未来”。