@大通福克斯美国会诊中心(CMAA)译
2017年9月11日下午,Caris在备受瞩目的2017欧洲肿瘤学会年会(ESMO2017)进行了主题发言,发言题目为“原发灶不明癌症应答免疫检查点阻断治疗的生物标志物综合分析”。在此,对于发言的重要信息为您带来最新的报道。

1、研究背景基于
原发灶不明肿瘤占所有恶性肿瘤的3%。常用肿瘤传导通路改变的检测将会对原发灶不明肿瘤患者采取分子靶向治疗提供合理的意见。逃避免疫破坏是新近发现的常见恶性肿瘤的一大特性。本研究对免疫检查点阻滞相关的生物标记物进行了深入探讨。
2、研究方法
本研究对389例原发灶不明肿瘤进行了592基因的下一代基因测序。仅使用非同义错义突变计算肿瘤突变负荷。对测序基因的目标区域直接进行已知的微卫星不稳定检测。阿切尔基因融合检测法用以进行基因融合检测,并分析156种肿瘤的52个基因靶点。免疫组化法用来检测肿瘤PD-L1的表达。所有以上检测均在CLIA、CAP及ISO认证的实验室进行。
3、研究结果
(1) 389名原发灶不明肿瘤患者,其中186名男性,203名女性。年龄范围为18-90岁,平均年龄为62.7岁。腺癌最多有175例,肿瘤类型不明确的有120例,鳞状细胞癌有30例,非小细胞肺癌有15例,粘液癌14例,神经内分泌癌9例,肉瘤样和梭形细胞癌8例,癌肉瘤2例,多形性细胞癌2例,浆液癌2例,硬戒细胞癌2例,罕见类型肿瘤10例。如下图:

(2) 对7例存在高度微卫星不稳定状态的原发灶不明肿瘤进行了分子图谱分析:其中5例出现了MSH2/MSH6或MSH1/PMS2未表达。另一例仅出现PMS2未表达。还有一例(#3)无法评估。具体如下图:
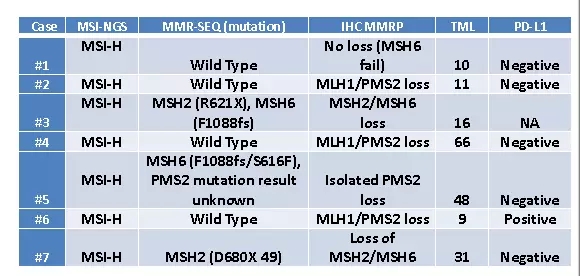
(3) 原发灶不明肿瘤表达高度肿瘤突变负荷、高度微卫星不稳定和PD-L1阳性的相关性评价:通过维恩图,我们发现在所进行的389例试验中,没有1例同时出现以上的3种分子标记状态。
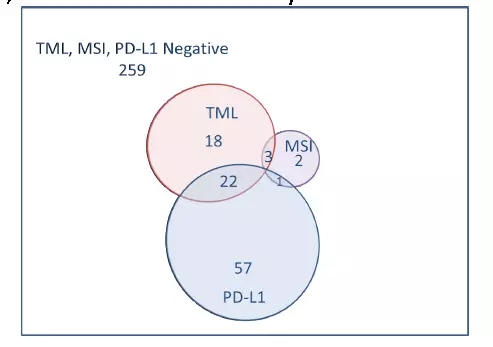
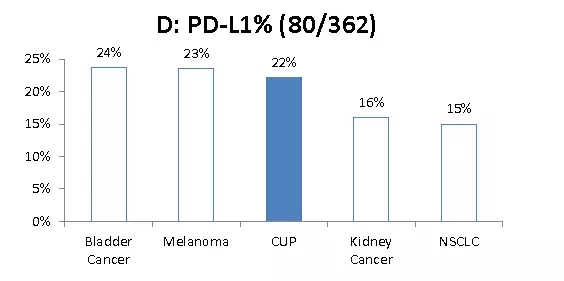
(4) 比较原发灶不明肿瘤和4种对免疫检查点阻滞剂敏感肿瘤(非小细胞肺癌NSCLS、膀胱癌Bladder、黑色素瘤Melanoma和肾癌Kidney)表达高度肿瘤突变负荷、高度微卫星不稳定和PD-L1阳性的比例。
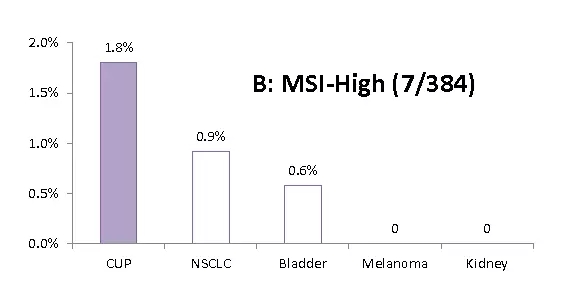
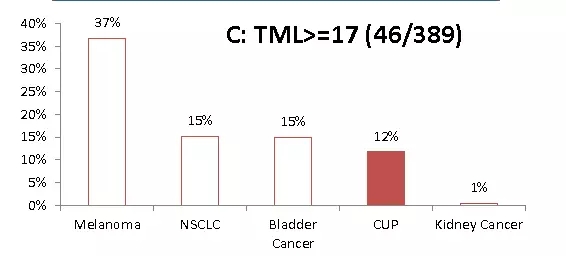
(5) 共有70种基因突变被检测出来,突变频率在0.3%到54%。下图列出本次研究突变频率在1%以上的突变基因:

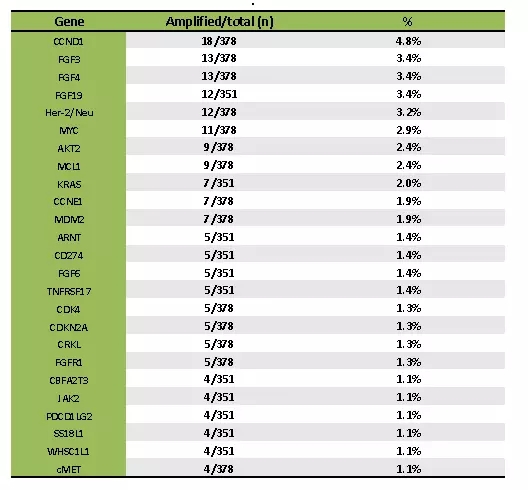
(6) 本项研究中检测到基因扩增频率大于1%的结果,如下图:
4、结论
(1) 本项研究表明相当大比例的原发灶不明肿瘤有潜力采用免疫检查点阻滞治疗,并且最近有报道证实对其中2位原发灶不明肿瘤患者治疗有效3,4。
(2) 通过多平台、多方法的生物标记物检测显示28%的原发灶不明肿瘤具有采取免疫检查点阻滞治疗的可能。
(3) 检测到的常见基因突变与先前报道结果一致1,2,比如TP53、KRAS、ARID1A、PTEN。
(4) 几种基因扩增包括CCND1、FGF3、FGF4、FGF19、HER2、MYC和AKT2,可考虑用于分子靶向治疗。
(5) 基因融合不仅能够改变诊断结果,还能够为原发灶不明肿瘤提供潜在可能的治疗靶点。
参考文献:
1、Gatalica, et al. Comprehensive tumor profiling identifies numerous biomarkers of drug response in cancers of unknown primary site: Analysis of 1806 cases. Oncotarget 2014;5:12440–12447.
2、Ross, et al. Comprehensive Genomic Profiling of Carcinoma of Unknown Primary Site: New Routes to Targeted Therapies. JAMA Oncol 2015;1:40-49.
3、Kato, et al. Utility of Genomic Analysis In Circulating Tumor DNA from Patients with Carcinoma of Unknown Primary. Cancer Res 2017;77:4238-4246.
4、Gröschel S. et al. Integration of genomics and histology revises diagnosis and enables effective therapy of refractory cancer of unknown primary with PDL1 amplification. Spring Harb Mol Case Stud. 2016; 2(6): a001180







